چکیده
در این مطالعه تأثیر ذرات نانومتری ZrO₂ بر ریزساختار، تراکمپذیری و مقاومت به هیدراتاسیون دیرگدازهای منیزیت–دولومیت بررسی شد. مقادیر ۰، ۲، ۴، ۶ و ۸ درصد وزنی ذرات ZrO₂ به دیرگدازهای منیزیت–دولومیت حاوی ۳۵ درصد وزنی CaO افزوده شد. مقاومت به هیدراتاسیون با اندازهگیری تغییر وزن نمونهها پس از ۷۲ ساعت در دمای ۲۵°C و رطوبت نسبی ۹۵٪ تعیین گردید.
نتایج نشان داد که با افزودن ذرات نانومتری ZrO₂، ثابت شبکهای CaO افزایش یافته، چگالی تودهای و مقاومت به هیدراتاسیون نمونهها افزایش یافت، در حالی که تخلخل ظاهری کاهش یافت. افزودن مقدار کم ZrO₂، تشکیل فاز CaZrO₃ را تسهیل کرد که باعث بهبود زینترینگ و فرآیند تراکمپذیری شد. مکانیسم تأثیر ذرات نانومتری ZrO₂ در بهبود تراکمپذیری و مقاومت به هیدراتاسیون، کاهش مقدار CaO آزاد در نمونهها است.
کلمات کلیدی: دیرگدازهای منیزیت-دولومیت، ذرات نانومتری ZrO₂، مقاومت به هیدراتاسیون، تراکمپذیری.
۱. مقدمه
دیرگدازهای منیزیت-دولومیت به دلیل دمای دیرگدازی بالا، دسترسی گسترده به مواد خام، مقاومت عالی در برابر سربارههای قلیایی و توانایی حذف ناخالصیها از فولاد مذاب، توجه گستردهای را به خود جلب کردهاند [۱-۵]. با این حال، حساسیت به هیدراتاسیون این دیرگدازها یک عیب عمده است که کاربردهای عملی آنها را محدود میکند [۱-۷]. روشهای بهبود مقاومت به هیدراتاسیون دیرگدازهای منیزیت-دولومیت شامل افزایش تراکمپذیری با افزودن کمکسینترکنندههایی مانند Fe₂O₃ ،Al₂O₃ ، CuO ، V₂O₅ ۱۲ و TiO₂ است. استفاده از Fe₂O₃، Al₂O₃، CuO و V₂O₅ به عنوان کمکذوبساز میتواند زینترینگ آهک و متعاقباً مقاومت به هیدراتاسیون دیرگدازهای منیزیت-دولومیت را بهبود بخشد. [با این حال، مذاب تشکیل شده ممکن است دمای دیرگدازی و مقاومت به سرباره دیرگداز را بهطور قابل توجهی کاهش دهد . رویکرد دیگر، کربناسیون سطحی و پوشش فسفاتی است. گزارش شده است که افزودن ZrO₂ میتواند مقاومت به هیدراتاسیون دیرگدازهای MgO-CaO را با بهبود زینترینگ حالت جامد بدون کاهش دمای دیرگدازی از طریق تشکیل محلولهای جامد مقاوم به هیدراتاسیون بهبود بخشد، اما باعث افزایش هزینه تولید میشود [۵, ۷, ۱۴ و ۱۵]. بنابراین، کاهش مقدار ZrO₂ به منظور بهبود خواص دیرگدازهای منیزیت-دولومیت مهم است. گزارش شده است که مقاومت به هیدراتاسیون دیرگدازها با پراکندگی مناسب ذرات نانومتری در ریزساختار بهطور محسوسی بهبود مییابد [۵, ۷]. هدف از کار حاضر، مطالعه تأثیر افزودن ذرات نانومتری ZrO₂ بر خواص دیرگدازهای منیزیت-دولومیت و نشان دادن امکان بهبود خواص این دیرگدازها با مقادیر کمتر ذرات نانومتری ZrO₂ است.
۲. روش آزمایشی
آنالیز شیمیایی دولومیت و منیزیت سینتر شده (در ۱۷۰۰°C) (به ترتیب مشتق از معادن زفره و بیرجند) در جدول ۱ نشان داده شده است. ترکیبات حاوی ۳۵ درصد وزنی CaO با ۲، ۴، ۶ و ۸ درصد وزنی نانو ZrO₂ (جدول ۲ و شکل ۱) (محصول شرکت Inframat Advanced Materials Co) مخلوط و سپس با پرس تکمحوری در ۹۰ مگاپاسکال فشرده شدند. بریکتهای خام در دمای ۱۱۰ ±۵°C به مدت ۲۴ ساعت خشک و در دمای ۱۶۵۰°C با زمان نگهداری ۳ ساعت در دمای اوج سینتر شدند. سینترینگ در کوره الکتریکی انجام شد و نرخ حرارتدهی تا ۱۱۰۰°C معادل ۵°C/min و سپس تا دمای سینترینگ نهایی معادل ۳°C/min حفظ شد. چگالی تودهای (BD) و تخلخل ظاهری (AP) نمونهها با استفاده از روش جابجایی مایع با اصل ارشمیدس در محیط زایلن تعیین شد. مقاومت به هیدراتاسیون به شرح زیر تعیین شد: هر نمونه پودر شد تا اندازه ذرات ریزتر از الک شماره ۴۰ (۴۲۵ میکرومتر) به دست آید. پس از توزین، آنها در ظرف پتری در اتوکلاو با رطوبت ۹۵% در دمای ۲۵°C قرار داده شدند. سپس نمونهها در زمانهای مختلف تا ۷۲ ساعت توزین شدند. ریزساختار با استفاده از میکروسکوپ الکترونی روبشی (SEM، Cambridge، S360) مجهز به واحد EDS سیستم ۵۴۸۰ IXRF بررسی شد. فازهای موجود در محصول سینتر شده با مطالعه پراش پرتو ایکس (XRD) (Jeol-8030، Cu-Kα و ۲۵ کیلوولت انجام شد.
جدول ۱. آنالیز شیمیایی منیزیت و دولومیت مورد استفاده در این مطالعه
|
اکسید |
منیزیت (% وزنی) |
دولومیت (% وزنی) |
|
MgO |
93.2 |
37.2 |
|
CaO |
2.7 |
57.7 |
|
TiO₂ |
0.2 |
0.2 |
|
MnO |
0.45 |
0.18 |
|
Fe₂O₃ |
0.6 |
0.6 |
|
Al₂O₃ |
1.6 |
2.8 |
|
SiO₂ |
0.8 |
0.7 |
|
L.O.I |
0.3 |
0.44 |
|
اندازه (µm) |
<80 |
<75 |
جدول ۲. مشخصات نانو ZrO₂
|
ذره |
اندازه متوسط ذره |
سطح ویژه (m²/g) |
خلوص (%) |
|
نانو-ZrO₂ |
۳۰±۳۵ نانومتر |
۱۶۰ |
> 99.9 |

شکل ۱. تصویر TEM از نانوذرات ZrO₂.
۳. نتایج و بحث
۳.۱. تراکمپذیری
آنالیز شیمیایی دولومیت و منیزیت مورد استفاده به عنوان مواد اولیه در جدول ۱ نشان داده شده است. همانطور که مشخص است، دولومیت و منیزیت مورد استفاده در این مطالعه دارای ناخالصیهایی مانند SiO₂، TiO₂، Al₂O₃ و Fe₂O₃ هستند. مقدار Al₂O₃ بیشتر از سایر ناخالصیها است. شکل ۲ تأثیر افزودن نانو ZrO₂ را بر چگالی تودهای و تخلخل ظاهری نمونههای سینتر شده در ۱۶۵۰°C به مدت ۳ ساعت نشان میدهد.
مشاهده میشود که چگالی تودهای بهتدریج افزایش و تخلخل ظاهری با افزودن نانو ZrO₂ کاهش مییابد. هنگامی که مقدار نانو ZrO₂ به ۸ درصد وزنی افزایش یافت، چگالی تودهای به ۳.۱۶ گرم بر سانتیمتر مکعب افزایش و تخلخل ظاهری به ۱۶.۸٪ کاهش یافت. از این نتایج مشخص میشود که افزودن نانو ZrO₂ تراکمپذیری دیرگدازهای منیزیت-دولومیت را بهبود بخشید. افزودن نانو ZrO₂ به دلیل تشکیل ذرات CaZrO₃ که یک فاز با انبساط حجمی است و تخلخل در ماتریس را کاهش میدهد، تراکمپذیری را بهبود داد.
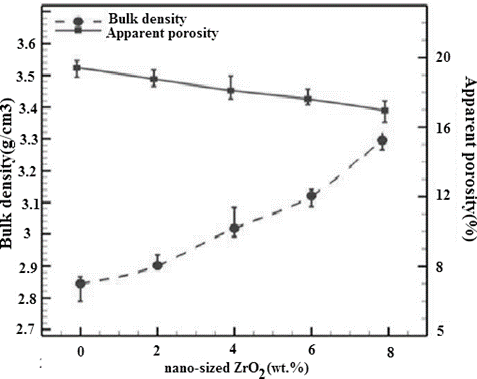
شکل ۲. تأثیر افزودن ذرات نانومتری ZrO₂ بر تراکمپذیری دیرگدازهای منیزیت-دولومیت.
۳.۲ آنالیزXRD
شکلهای ۳ و ۴ الگوهای XRD نمونههای با و بدون افزودن نانو ZrO₂ را نشان میدهند. پریکلاز (MgO) و آهک (CaO) فازهای کریستالی اصلی در همه نمونهها بودند و حضور Al₂O₃ به عنوان ناخالصی در مواد اولیه، باعث تشکیل فاز Ca₃Al₂O₆ شد.
در نمونههای حاوی ۲ و ۸ درصد وزنی نانو ZrO₂، MgO، CaO و CaZrO₃ فازهای کریستالی اصلی بودند و هیچ اثری از فاز نانو ZrO₂ مشاهده نشد. این نشان میدهد که تمام نانو ZrO₂ افزوده شده با CaO واکنش داده و فاز CaZrO₃ را تشکیل داده است. هیچ تغییری در پارامتر شبکه فاز MgO هنگام افزودن نانو ZrO₂ اندازهگیری نشد. این نشان میدهد که نانو ZrO₂ با فاز MgO محلول جامد تشکیل نداد. موقعیت پیکهای پراش مربوط به CaO در نتیجه افزودن نانو ZrO₂ جابجا شد، که نشان میدهد Zr⁴⁺ وارد شبکه CaO شده و پارامتر شبکه آن را تغییر داده است. با این حال، هیچ تغییری در موقعیتهای MgO مشاهده نشد. ثابت شبکه CaO در نمونهها (جدول ۳) با مقایسه موقعیت پیکها (۲θ) الگوهای XRD و با استفاده از روش حداقل مربعات تعیین شد.
ثابت شبکه CaO در نمونههای بدون ZrO₂ ۴.۷۹۷۸ آنگستروم یافت شد [۷, ۱۴, ۱۶] که با ثابت شبکهای CaO خالص مطابقت داشت [۷]. افزودن نانو ZrO₂ ثابت شبکه CaO را افزایش داد. هنگامی که مقدار ZrO₂ افزوده شده ۸ درصد وزنی بود، ثابت شبکه CaO به بالاترین مقدار خود در αCaO = ۴.۸۹۷۲ آنگستروم رسید. به طور کلی، محلول جامد اکسیدهای فلزی عمدتاً با جایگزینی کاتیونها در حلال تشکیل میشود. شعاع کاتیونها مستقیماً بر انرژی پیوند کاتیونها و آنیونها در بلورهای یونی تأثیر میگذارد و در نتیجه بر حلالیت جامد تأثیر میگذارد. هنگامی که اختلاف شعاع کاتیونها کمتر از ۱۵٪ باشد، تشکیل محلول جامد آسان است؛ هنگامی که اختلاف بیشتر از ۳۰٪ باشد، تشکیل محلول جامد امکانپذیر نیست [۷]. در این مطالعه، اختلاف شعاع بین Ca²⁺ (۰.۰۹۹ نانومتر) و Zr⁴⁺ (۰.۰۹۸ نانومتر) [۲, ۷] حدود ۱٪ بود، اما اختلاف شعاع بین Mg²⁺ (۰.۰۷۲ نانومتر) [۷] و Zr⁴⁺ نزدیک به ۳۶٪ بود. بنابراین، انتظار میرود نانو ZrO₂ به راحتی در CaO حل شود اما در MgO حل نشود که این موضوع توسط نتایج آنالیز XRD تأیید شد.
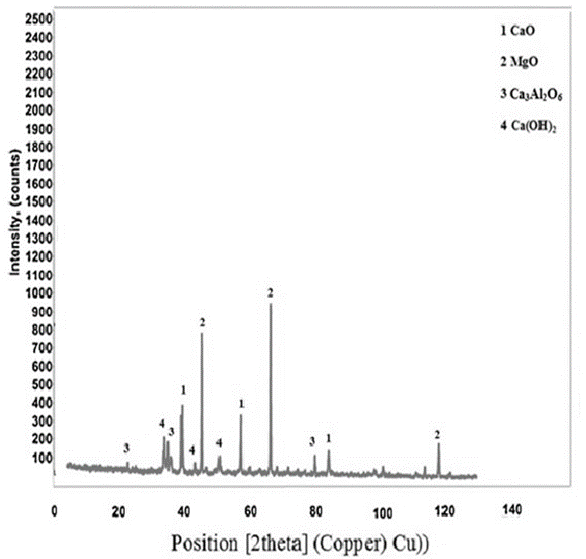
شکل ۳. الگوی XRD نمونه بدون ZrO₂.
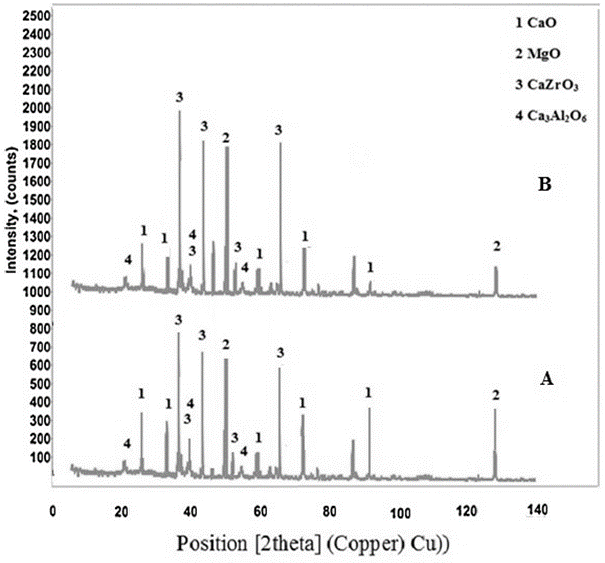
شکل ۴. الگوهای XRD نمونههای حاوی: الف) ۲ درصد وزنی و ب) ۸ درصد وزنی ZrO₂.
جدول ۳. ثابت شبکهای محاسبه شده برای نمونههای سینتر شده
|
نمونه |
پارامترها |
۱۱۱ |
۲۰۰ |
۲۲۰ |
۳۱۱ |
۲۲۲ |
a(Å) |
|
بدون ZrO₂ |
2θ(°) |
31.31 |
37.51 |
53.4 |
63.54 |
67.08 |
4.7978 |
|
d(Å) |
1.654 |
2.382 |
1.678 |
1.457 |
1.387 |
||
|
۲% وزنی ZrO₂ |
2θ(°) |
31.45 |
37.45 |
53.39 |
64.37 |
67.45 |
4.8023 |
|
d(Å) |
2.674 |
2.3842 |
1.674 |
1.457 |
1.347 |
||
|
۴% وزنی ZrO₂ |
2θ(°) |
31.47 |
37.39 |
54.06 |
64.62 |
67.47 |
4.8544 |
|
d(Å) |
2.745 |
2.377 |
1.701 |
1.444 |
1.358 |
||
|
۶% وزنی ZrO₂ |
2θ(°) |
32.37 |
37.89 |
54.09 |
64.66 |
67.54 |
4.8871 |
|
d(Å) |
2.761 |
2.387 |
1.712 |
1.478 |
1.384 |
||
|
۸% وزنی ZrO₂ |
2θ(°) |
32.88 |
37.92 |
54.12 |
64.87 |
67.66 |
4.8972 |
|
d(Å) |
2.774 |
2.701 |
1.725 |
1.502 |
1.398 |
۳.۳. مقاومت به هیدراتاسیون
شکل ۵ تأثیر افزودن نانو ZrO₂ را بر مقاومت به هیدراتاسیون دیرگدازهای منیزیت-دولومیت نشان میدهد. مشاهده میشود که افزایش جرم نمونههای منیزیت-دولومیت با افزودن نانو ZrO₂ بهطور محسوسی کاهش یافت. برای نمونه بدون افزودنی، افزایش جرم پس از ۷۲ ساعت ۱.۸۲٪ بود که با افزایش مقدار ZrO₂ بهشدت کاهش یافت. افزایش جرم با افزودن ۸٪ نانو ZrO₂ به ۱.۴۲٪ کاهش یافت که نشاندهنده بهبود مقاومت به هیدراتاسیون با افزودن نانو ZrO₂ است. مشخص است که مقاومت به هیدراتاسیون مواد حاوی CaO، اعم از مواد غنی از CaO و غنی از MgO، به شدت به محتوای CaO و ریزساختار وابسته است. هنگامی که نانو ZrO₂ افزوده میشود، افزایش مقاومت به هیدراتاسیون دیرگدازها به دلایل زیر در نظر گرفته میشود: اول، با تبدیل بخشی از CaO آزاد به CaZrO₃ بدون آب. با افزایش افزودن نانو ZrO₂، محتوای CaO آزاد در دیرگدازها بیشتر کاهش یافته و در نتیجه مقاومت به هیدراتاسیون دیرگدازها بهبود یافت. دوم، بهبود تراکمپذیری با افزودن نانو ZrO₂ تخلخل دیرگدازها را کاهش داد. سوم، مقاومت به هیدراتاسیون دیرگدازها با اصلاح ریزساختار بهبود یافت.
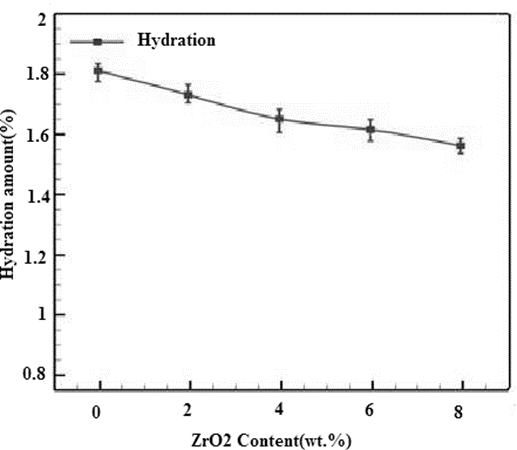
شکل ۵. تأثیر افزودن نانو ZrO₂ بر بهبود مقاومت به هیدراتاسیون نمونهها.
۳.۴. آنالیز SEM
شکل ۶ ریزساختار نمونههای بدون و حاوی مقادیر مختلف نانو ZrO₂ را نشان میدهد. نمونه سینتر شده بدون افزودن نانو ZrO₂ دارای تخلخل بیشتر و دانههای بزرگتر در مقایسه با نمونههای حاوی نانو ZrO₂ است. تشکیل فاز CaZrO₃ (جدول ۴) با مهار رشد دانه در CaO و MgO همراه بود. رشد دانه CaO به دلیل دشواری انتشار یونهای Ca²⁺ در سراسر ماتریس در طول فرآیند زینترینگ، مهار شد. مشاهده میشود که تعداد تخلخلها با افزایش محتوای نانو ZrO₂ تا ۸ درصد وزنی بهتدریج کاهش یافت. همچنین میتوان خاطرنشان کرد که تخلخلها در مرزهای بین دانههای MgO و CaO وجود داشتند. تعداد تخلخلها در مرز دانهها در طول فرآیند زینترینگ در نتیجه مهاجرت مرز دانه کاهش مییابد که منجر به تشکیل تخلخلهای بزرگتر روی سطح کریستال میشود که ممکن است با پیشرفت فرآیند زینترینگ حذف شوند.
شکل ۶. تصاویر SEM از سطوح شکست نمونههای: الف) بدون، ب) ۲٪، ج) ۶٪ و د) ۸٪ وزنی نانو ZrO₂.

جدول ۴. آنالیز EDS نقطهای در شکل ۶d که تشکیل فاز CaZrO₃ را تأیید میکند.
|
عنصر |
O |
Mg |
Ca |
Zr |
|
% وزنی |
24.91 |
0.52 |
41.74 |
32.83 |
|
% اتمی |
45.87 |
0.62 |
27.36 |
26.15 |
یک توضیح احتمالی برای تأثیر نانو ZrO₂ بر تراکمپذیری و مقاومت به هیدراتاسیون دیرگدازهای MgO-CaO شامل یک فرآیند انحلال است که در آن کاتیونهای Zr⁴⁺ به CaO (MgO) افزوده میشوند تا محلول جامد مطابق معادله ۱ تشکیل دهند:
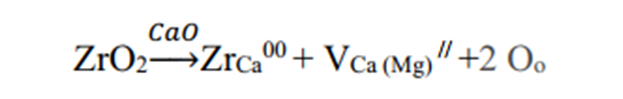
نکته اصلی در واکنش (۱)، تشکیل نقصهای خالی (واکنی) کلسیم یا منیزیم در واکنش (۱) است. تشکیل نقصهای خالی میتواند تأثیر مثبتی بر فرآیند تراکمپذیری داشته باشد. این اثرات چگالی پودر را افزایش داده و مقاومت به هیدراتاسیون دیرگدازهای منیزیت-دولومیت را بهبود میبخشد. ترجیح کاتیونهای Zr⁴⁺ برای تشکیل محلول جامد با CaO را میتوان از ساختار بلوری توضیح داد. اگرچه MgO و CaO هر دو در ساختار مکعبی نمک سنگ یکسان متبلور میشوند، پیوند Mg-O دارای استحکام تک پیوندی بالاتر (۱.۵۵ × ۱۰⁵ ژول بر مول) نسبت به پیوند Ca-O (۱.۳۳ × ۱۰⁵ ژول بر مول) است که به دلیل شعاع کوچکتر کاتیون Mg²⁺ (۰.۰۷۸ نانومتر) در مقایسه با کاتیون Ca²⁺ (۰.۱۰۰ نانومتر) است [۲, ۷ و ۱۴].
۴. نتیجهگیری
افزودن ذرات نانومتری ZrO₂ تراکمپذیری را به دلیل تشکیل ذرات CaZrO₃ که یک فاز با انبساط حجمی ناشی از واکنش ZrO₂ افزوده شده با CaO در دیرگدازهای منیزیت-دولومیت است، بهبود بخشید.
کاتیونهای Zr⁴⁺ ترجیح میدهند با CaO محلول جامد تشکیل دهند؛ بهبود مقاومت به هیدراتاسیون CaO-MgO از طریق کاهش غلظت Ca²⁺ در CaO حاصل شد.
مقاومت به هیدراتاسیون دیرگدازهای منیزیت-دولومیت با تبدیل بخشی از CaO آزاد به CaZrO₃ بدون آب بهبود یافت.
بهبود تراکمپذیری با افزودن ZrO₂ تخلخل دیرگدازها را کاهش داد و در نتیجه سطح واکنش ویژه آنها هنگام قرار گرفتن در معرض محیط مرطوب کاهش یافت.
مراجع
[1] Kashaninia, F., Sarpoolaky, H., Naghizadeh, R., Bagheri, A. R. and Zamanipour, M., "Improving Hydration Resistance of Magnesia-Doloma Refractories by Iron Oxide Addition", Iran. J. Mat. Sci. Eng., 2011, 8, 4.
[2] Zhang, H., Zhao, H., Zhen, J., Yu, j. and Nie, J., "Defect Study of MgO-CaO Material doped With CeO₂". J. adv. Mat. Sci. eng, 2013, 20, 1-5.
[3] Kahrizsangi, S. Gh., Nemati, A., Shahraki, A. and Farooghi, M., "Effect of Nano-Sized Fe₂O₃ on Microstructure and Hydration Resistance of MgO-CaO Refractories", Int. J. Nanosci. Nanotech., 2016, 12, 19-26.
[4] Kahrizsangi, S. Gh., Shahraki, A. and Farooghi, M., "Effect of Nano-TiO₂ Additions on the Densification and Properties of Magnesite-Dolomite Ceramic Composite", Irani. J. Sci. Tech. Tran. A, 2016, 1-9.
[5] Chen, M., Lu, C. and Yu, J., "Improvement in performance of MgO-CaO refractories by the addition of nano-sized ZrO₂". J. Eur. Ceram. Soc, 2007, 27, 4633-4638.
[6] Kahrizsangi, S. Gh, Nemati, A., Shahraki, A. and Farooghi, M., "Densification and properties of Fe₂O₃ nanoparticles added CaO refractories", Ceram. Int, 2016, 42, 12270-12275.
[7] Kahrizsangi, S. Gh., Nemati, A., Shahraki, A. and Farooghi, M, "The Effect of Nano-Additives on the Hydration Resistance of Materials Synthesized from the MgO-CaO System". Int. J. Eng., 2016, 29.
[8] Koval. E. J., Messing, G. L. and Bradt, R., "Effects of raw material properties and Fe₂O₃ additions on the sintering of dolomites", Ceram. Bull., 1984, 63, 274-277.
[9] Yeprem, "Effect of iron oxide addition on the hydration resistance and bulk density of doloma", J. Eur. Ceram. Soc, 2007, 1651-1655.
[10] Cho, Ch. H., Goo, B. J., Lee, K. S. and Kim, D. K., "Effect of Al₂O₃, MgO and SiO₂ on sintering and hydration behaviours of CaO ceramics", j. Korean. Ceram. Soc. 2002, 39, 528-534.
[11] Ghosh, A., Bhattacharay, T. K., Mukherjee, B. and Das, S. K., "The effect of CuO addition on the sintering of lime", J. Ceram. Int, 2011, 27, 201-203.
[12] Ghosh, A., Bhattacharay, T., Mukherjee, B. and Das, S. K., "Densification and properties of lime with V₂O₅ additions", J. Ceram. Int, 2004, 30, 2117-2120.
[13] Chen, M., Wang, N., Yu, J. and Yamaguchi, A., "Effect of Porosity on Carbonation and Hydration of CaO Material". J. Eur. Ceram Soc, 2007, 27, 1953-1959.
[14] Pang, C., Li, N. and Han, B., "Effect of zircon on sintering, composition and microstructure of magnesia powder, J. sci. sint, 2009, 41, 11-17.
[15] Chen, M., Lu, C. Y. and Yu, J. K., "Sintering and performance of MgO-CaO materials with Nano-sized ZrO₂ addition", Mat. Sci. foru, 2007, 561, 623-626.
[16] Gionea, A., Andronescu, E., Voicu, G., Vasile-Surdu A. and Ilie, A., "ZrO₂-CaO Ceramics -- A Comparative Study", U. P. B. Sci. Bull., 2016, 78, 1.

 FA
FA  EN
EN  AR
AR 