چکیده
در این مطالعه، دولومایت طبیعی خالص (بدون افزودنی) و پوسته آسیاب (با محتوای ۹۸.۶۶ درصد وزنی Fe2O3) اضافه شده (تا ۱.۵ درصد وزنی) از سلجوقلو-کونیا ترکیه با استفاده از فرآیند یک مرحلهای در دمای ۱۶۰۰-۱۷۰۰ درجه سانتیگراد به مدت ۲ تا ۶ ساعت پخته شد. چگالی حجمی حاصل و تخلخلهای ظاهری دولومای زینترینگ شده بررسی شد.
طبق نتایج آزمایشها با ۱۵ نمونه زینترینگ شده، مشخص شد که دمای زینترینگ، زمان خیساندن و افزایش مقدار پوسته آسیاب، چگالی حجمی را افزایش داده و در نتیجه تخلخل ظاهری مشاهده شده را کاهش میدهد. در آزمایشهای مقاومت در برابر هیدراتاسیون، به نظر میرسید که همین ویژگیها مقاومت را نیز افزایش میدهند. علاوه بر این، آنالیز EDX دولومایی که در سه دمای مختلف، هر کدام با 0.5 درصد وزنی پوسته آسیاب و همچنین در دمای 1700 درجه سانتیگراد بر 2 ساعت با 0 تا 1 درصد وزنی پوسته آسیاب، تف جوشی شده بودند، انجام شد. مقادیر Fe2+،3+ در داخل پریکلاز (MgO) بررسی شد. چگالی حجمی دولومای خالص (CaO·MgO) با استفاده از مقادیر چگالی CaO خالص و MgO که در مقالات ارائه شده است، محاسبه شد. تفاوت بین مقدار برونیابی شده چگالیهای اندازهگیری شده و چگالی حجمی دولومایی که از دادههای مقالات بدون تخلخل محاسبه شده است، بسیار نزدیک است.
- مقدمه
دولومایت با ترکیب شیمیایی ایدهآل CaMg(CO₃)₂ یک ماده اولیه دیرگداز است. دولوما، محصول حاصل از کلسیناسیون دولومایت، شامل مخلوطی از آهک (CaO) و پریکلاز (MgO) است. نقطه ذوب یوتکتیکی سیستم دوتایی CaO–MgO برابر با 2370°C است. دولوما به شدت مستعد آبدیدگی است و بنابراین نسبت آهک آزاد در آن باید کمتر از حد بحرانی باشد. برای استفاده صنعتی، چگالی حجمی باید بالای 3 g/cm³ باشد.
اکسیدهای ناخالصی مانند SiO₂، Al₂O₃ و Fe₂O₃ به صورت معمول در دولومایت وجود دارند. نوع و مقدار این اکسیدها نقش مهمی در زینتر ایفا میکند و میتوانند زینتر را از طریق مکانیسم فاز مایع فعال کنند. اکسید آهن بهویژه به دلیل تولید فازهایی با نقطه ذوب پایین مانند C₄AF و C₂F، زینتر را تقویت کرده و همچنین مقاومت در برابر آبدیدگی را افزایش میدهد. همچنین افزودن Fe₂O₃ موجب افزایش چگالی حجمی میشود. دولومای زینترشده حاوی Fe₂O₃ را معمولاً "دولوما سوخته کامل" یا Dead Burnt Doloma مینامند.
برخی پژوهشها نیز نشان دادهاند که مقادیر بالاتر از 1.7٪ Fe₂O₃ تأثیر چندانی بر چگالی ندارد. در شرایط عادی، Fe₂O₃ تا 35٪ در MgO محلول است و باعث رشد دانههای پریکلاز و تبدیل آن به فاز مگنزیو-وستیت [(Mg,Fe)O] میشود. این رشد دانه موجب افزایش مقاومت در برابر آبدیدگی میگردد.
- روش آزمایش
میانگین اندازه دانه دولومایت استخراج شده از یک ذخیره دولومایت که محلی است و قبلاً برای صنعت نسوز استفاده نمیشد، با گرفتن یک مقطع نازک در آنالیز تصویر میکروسکوپ نوری LEICA Q 550 CW، 200 میلیمتر تعیین شد و پس از آنالیز شیمیایی مرطوب، در محدوده کسری 3 تا 6 میلیمتر دانهبندی شد. ترکیب دولومایت در جدول 1 آورده شده است. مخلوط طبیعی و 0.5 تا 1.5 درصد وزنی مقیاس آسیاب (98.66 درصد وزنی Fe2O3 زیر 45 میلیمتر) با استفاده از آب مقطر به عنوان ماده اتصال دهنده تولید شد.6 سپس آنها در بوتههای منیزیت خالص قرار داده شدند و به مدت 2 ساعت در دمای 110 درجه سانتیگراد خشک شدند و با سرعت گرمایش 10 درجه سانتیگراد در دقیقه، به مدت 2 تا 6 ساعت در محدوده دمایی 1600 تا 1700 درجه سانتیگراد تف جوشی شدند. پس از آن، چگالی ظاهری و مقاومت هیدراتاسیون دولومای بهدستآمده اندازهگیری شد. آزمایشها در هوا و در یک کوره آزمایشگاهی با المنتهای گرمایشی MoSi2 انجام شد. شرایط پخت، چگالی ظاهری، تخلخلهای ظاهری و نتایج مقاومت هیدراتاسیون در جدول 2 نشان داده شده است. چگالی ظاهری و تخلخل ظاهری دولوماها با روش «ارشمیدس» و با استفاده از محیط الکل اتیل اندازهگیری شد.
جدول 1: ترکیب شیمیایی دولومایت مورد استفاده در این مطالعه (بدون از دست دادن اشتعال)
|
ترکیب |
درصد وزنی |
|
CaO |
29.46 |
|
MgO |
22.52 |
|
SiO₂ |
0.15 |
|
Al₂O₃ |
0.15 |
|
Fe₂O₃ |
0.04 |
جدول2: تغییرات چگالی ظاهری، تخلخل ظاهری و درجه هیدراتاسیون به دلیل شرایط پخت دولوما
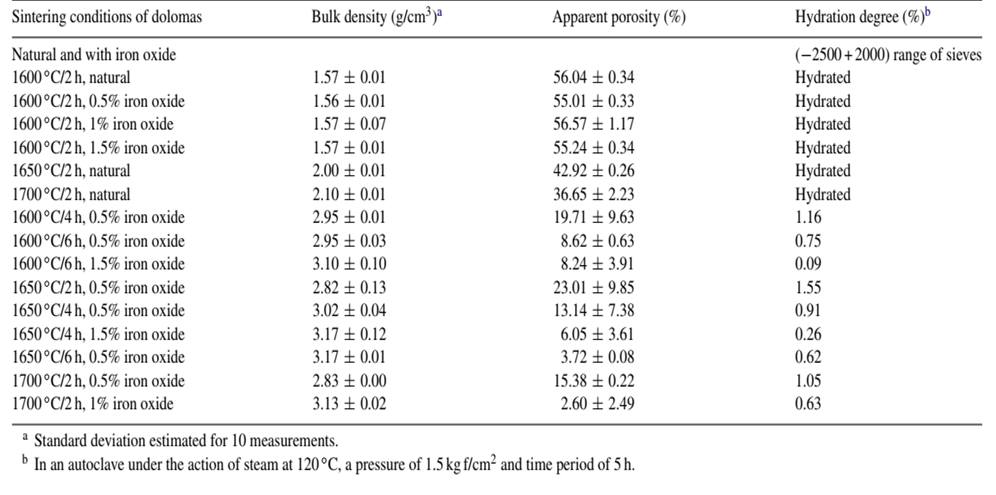
دولوماها در رزین اکریلیک مانت شده و سپس با SiC از 320 تا 1000 گریت در حضور اتیل الکل ساییده شدند. صیقل دادن نمونه با خمیر الماس 3 میلیمتری انجام شد. در طول آمادهسازی نمونه، از آب استفاده نشد زیرا فاز آهک به سرعت هیدراته میشود و باعث ایجاد ترک در دانههای آهک ریزساختار دولوما میشود. مقادیر Fe2+،3+ در پریکلاز موجود در دولوما با سه افزودن مختلف در محدوده 0 تا 1 درصد وزنی در دمای 1700 درجه سانتیگراد/2 ساعت و با افزودن 0.5 درصد وزنی پوسته آسیاب در سه دمای مختلف با استفاده از SEM/EDX تعیین شد. حدود 25 تا 30 میکروآنالیز برای هر نمونه انجام شد و هر آنالیز گزارش شده در این مطالعه، میانگین مقدار سه آنالیز انجام شده در پریکلاز است. آنالیز EDX با نادیده گرفتن O2 انجام میشود. ریزساختار برخی از نمونههای متراکم انتخابشده با استفاده از میکروسکوپ الکترونی روبشی Jeol JSM (SEM) مدل 5410 LV مجهز به واحد میکروآنالیز اشعه ایکس با پراکندگی انرژی (EDX) سیستم 5480 IXRF بررسی شد.
- نتایج و بحث
3.1چگالی حجمی و تخلخل
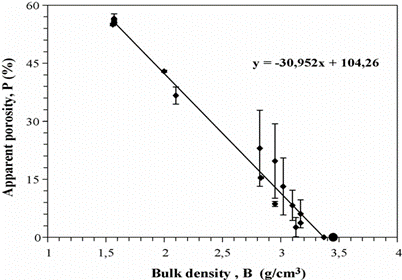
اثرات افزودن پوسته آسیاب و دمای زینترینگ بر چگالی حجمی دولوما در جدول 2 نشان داده شده است. همانطور که مشاهده میشود، افزودن پوسته آسیاب در شرایط 1600 درجه سانتیگراد/2 ساعت که در آن زینترینگ به صورت جزئی رخ میدهد، مؤثر نیست. با این حال، در گروههای دیگر مشاهده میشود که افزایش نسبت افزودن به همراه زمان و دما بر افزایش چگالی حجمی مؤثر است. افزایش چگالی حجمی نشان میدهد که زینترینگ رخ داده است؛ همچنین نشان میدهد که دمای زینترینگ کاهش یافته است. مشاهده میشود که این افزایش به ویژه بین افزودن 0 تا 0.5 درصد وزنی و در زینترینگ 1650 درجه سانتیگراد/2 ساعت بیشتر است. چگالی حجمی هنگام عبور از نمونه بدون افزودن به نمونه با افزودن 0.5 درصد وزنی تقریباً 41 درصد افزایش مییابد. این افزایش تقریباً تا 6٪ بین محدوده افزودن 0.5 تا 1 درصد وزنی ادامه مییابد و به ندرت افزایشی بین محدوده افزودن 1 تا 1.5 درصد وزنی مشاهده میشود. به نظر میرسد که مقادیر بهینه برای نسبت پوسته آسیاب در محدوده 0.5 تا 1 درصد وزنی است.
BMgO = 3.65 g/cm3، BCaO = 3.32 g/cm3. مقادیر 40.37 wt.% MgO و 59.63 wt.% CaO با در نظر گرفتن میانگین مقادیر آنالیز شیمیایی دولومای خالص مورد استفاده در مطالعه در سه دمای مختلف و با متعادل کردن آن تا 100٪ بدست آمدند.
در جدول 2 میتوانیم ببینیم که افزودن پوسته آسیابی، مقاومت در برابر هیدراتاسیون را تضمین میکند (به جز نمونههای زینترینگ شده در شرایط 1600 درجه سانتیگراد/2 ساعت که در آن زینترینگ رخ نمیدهد) پس از دماها و زمان مناسب که در آن زینترینگ رخ میدهد.
در آزمایش هیدراتاسیون نمونههایی با افزودن 0.5 و 1.5 درصد وزنی و زینترینگ شده در دمای 1650 درجه سانتیگراد/4 ساعت، مشاهده میشود که مقاومت نمونه با افزودن 1.5 درصد وزنی در برابر هیدراتاسیون تقریباً 200٪ بیشتر از نمونه با افزودن 0.5 درصد وزنی است.
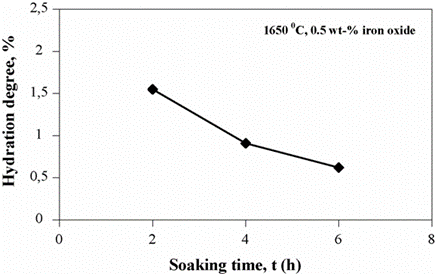
وضعیت مشابهی در نمونههای تحت شرایط زینترینگ 1600 درجه سانتیگراد/6 ساعت مشاهده میشود. با این حال، همانطور که میدانیم افزودن بیش از حد اکسید آهن منجر به فرسایش سرباره میشود33 و تأثیر این افزایش مقدار اکسید آهن بر چگالی حجمی - همانطور که در نتایج آزمایشها نیز مشاهده میشود - زیاد نیست، استفاده از پوسته آسیاب بیش از 0.5 درصد وزنی در عمل توصیه نمیشود. در شکل 2 مشاهده میشود که مقاومت هیدراتاسیون با افزایش زمان در محدوده دورههای پخت 2 تا 4 ساعته به سرعت افزایش مییابد و افزایش بیشتر با زمان مجانبی است. از دادههای ارائه شده در جدول 2 میتوان نتیجه گرفت که برای مقاومت هیدراتاسیون، افزایش زمان پخت مؤثرتر از افزایش دما است.
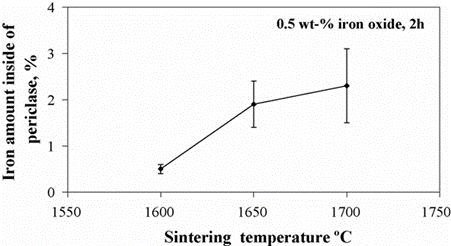
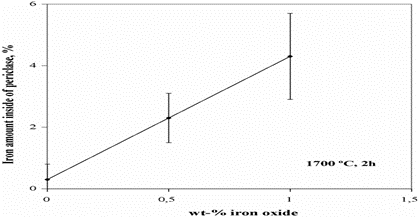
ریزساختارهای گرانولهای دولومای با افزودن 0.5 درصد وزنی پوسته آسیاب در شکل 3 برای سه دمای مختلف نشان داده شده است که در آنها رشد دانه مشهود است. تغییرات مقدار آهن پریکلاز در شکل 4 نشان داده شده است. مقدار آهن در پریکلاز با افزایش دما افزایش مییابد. این افزایش در محدوده دمایی پایینتر قابل توجه است و با افزایش دما کمتر میشود. پریکلاز رشد دانه را نشان میدهد و در طول رشد با افزایش دما به شکل منیزیووستیت در میآید و همچنین افزایش انرژی درونی آن با نفوذ آهن ایجاد میشود. این مقدار آهن به مقدار اکسید آهن در دولومای متصل است. افزایش خطی مقدار آهن در پریکلاز همراه با افزایش افزودن در مقیاس آسیاب در شکل 5 دیده میشود. در اینجا به راحتی میتوان مشاهده کرد که با افزایش نسبت افزودن، پریکلاز، به عبارت دیگر منیزیووستیت، آهن را با همان نسبت افزودن به ساختار خود جذب میکند. اگرچه محدوده افزودن 1 و 1.5 درصد وزنی مورد مطالعه قرار نگرفته است، اما تصور میشود که نسبت افزودن میتواند تأثیر کمی داشته باشد.
در مورد محتوای آهن پریکلاز، همانطور که روند مشابهی در مقادیر چگالی در همان محدوده افزودنی مشاهده شد.
شکل 1:رابطه چگالی ظاهری با تخلخل ظاهری.
شکل 2:رابطه زمان خیساندن با درجه هیدراتاسیون
شکل4:رابطه بین آهن موجود در پریکلاز و دما
شکل 5: رابطه بین آهن موجود در پریکلاز و میزان پوسته آسیاب
خلاصه نتایج حاصله شامل موارد زیر می باشد:
در دمای 1600°C/2h افزودن Fe₂O₃ تأثیر چندانی نداشت، اما در سایر شرایط، افزایش مقدار Fe₂O₃ و زمان ماند موجب افزایش چگالی حجمی شد.
- بیشترین افزایش چگالی از 0 تا 0.5٪ Fe₂O₃ دیده شد (~41)٪
- افزایش از 0.5 تا 1٪ منجر به حدود 6٪ رشد بیشتر شد
- افزایش از 1 به 1.5٪ تأثیر کمی داشت
مقدار بهینه Fe₂O₃: بین 0.5–1.0٪ وزنی
دانسیته دولوما از ترکیب وزنی CaO و MgO بدون تخلخل چنین محاسبه شد:
- MgO = 3.65 g/cm³
- CaO = 3.32 g/cm³
- محاسبه: B = 0.4037×3.65 + 0.5963×3.32 = 3.45 g/cm³
- مقدار تجربی: 3.37 g/cm³
- اختلاف: فقط 2.3٪
3.2 مقاومت در برابر آبدیدگی
مقدار آبدیدگی در شرایط مختلف در جدول زیر آمده است:
|
شرایط زینتر |
Fe₂O₃ (%) |
چگالی (g/cm³) |
تخلخل (%) |
درصد آبدیدگی |
|
1650°C/4h |
0.5 |
3.02 ± 0.04 |
13.14 |
0.91 |
|
1650°C/4h |
1.5 |
3.17 ± 0.12 |
6.05 |
0.26 |
نتیجه: مقاومت در برابر آبدیدگی با افزایش Fe₂O₃ بهطور قابلتوجهی افزایش یافت.
با این حال، به دلیل افزایش خوردگی سرباره در سطوح بالای Fe₂O₃، توصیه نمیشود بیش از 0.5٪ استفاده شود.
3.3 آنالیز ریزساختاری
- افزایش Fe در دمای بالاتر موجب رشد دانه پریکلاز شد
- در دمای بالاتر، آهن به شکل یکنواخت در فاز MgO نفوذ کرد و فاز [(Mg,Fe)O] (مگنزیو-وستیت) تشکیل شد
- افزایش Fe در پریکلاز با نسبت افزودهشده همبستگی خطی داشت
- نتیجهگیری
- افزودن Fe₂O₃ باعث افزایش چگالی و کاهش تخلخل شد
- آهن در فاز MgO نفوذ کرده و فاز مگنزیو-وستیت تشکیل داد
- افزایش اندازه دانه MgO منجر به افزایش مقاومت در برابر آبدیدگی شد
- شرایط زینتر بهینه و اقتصادی: 1650°C به مدت 4–6 ساعت با 0.5٪ Fe₂O₃
- دولومایت منطقه قونیه (ترکیه) پتانسیل مناسبی برای کاربرد در آجرهای دیرگداز دارد.
منابع
1. Chesters, J. H., Steelplant Refractories: Testing, Research and Development. The United State Com, Sheffield, 1963, 167
2. Trojer, F., Mineralogie Basissche Feurfest-Produkte. Springer-Verlag, New York, 1981, p. 42.
3. Anonymous, Didier Refractory Techniques—Refractory Materials and
Their Properties English Handbook, 1982, p. 41.
4. Routschka, G., Feuerfeste Werkstoffe. Vulkan Verlag, Essen, 1987.
5. O’Driscoll, M., Refractory dolomite. Ind. Miner., 1998, 6, 35–43.
6. Koval, E. J., Messing, G. L. and Bradt, R., Effects of raw material properties
and Fe2O3 additions on the sintering of dolomites. Ceram. Bull., 1984, 63,274–277.
7. Meyer, W., Franchi, A., Buchebner, G. and Willingshofer, M., The use of
dolomite-carbon-lined ladlesfor the production of superclean steels.VeitschRadex Rundschau, 1998, 2, 32–44.
8. Huppmann, W. J. and Riegger, H., Modelling of rearrangement processes
in liquid phase sintering. Acta Metall., 1975, 23, 965–971.
9. Kingery,W. D., Bowen, H. K. and Uhlmann, D. R.,Introduction to Ceramics.
John Wiley & Sons, New York, 1976.
10. Pask, J. A., Grain Boundaries in Sintering, Science of Sintering: New Directions for Materials Processing and Microstructural Control. Plenum Press,
New York, 1989.
11. Nan, L., Sintering of aggregated MgO powders. In Proceedings of the International Institute for the Science of Sintering (IISS) Symposium, 1987, pp.
346–351.
12. Bhattacharya, T. K., Ghosh, A. and Das, S. K., Densification of reactive lime
from limestone. Ceram. Int., 2001, 27, 455–459.
13. Yeprem, H. A., Turedi, E. and Karagoz, S., A quantitative-metallographic
study of the sintering behaviour of dolomite. Mater. Char., 2003, 52,331–340.
14. Oates, J. A. H., Lime and Limestone Chemistry and Technology. WileyVCH, USA, 1998, p. 150.
15. Boynton, R. S., Chemistry and Technology of Lime and Limestone. John
Wiley and Sons, New York, 1980.
16. Yeprem, H. A., Characterization of sintering of a local dolomite for production of dolomite refractory, PhD thesis, Yildiz Technical University, Istanbul,
Turkey, 2003.
17. Obst, K. H. and Munchberg, W., Mineralogical studies of dolomite as a basic ¨ refractory material. Br. Ceram. Soc., 1979, 6, 225–241.
18. Nishikawa, A., Technology of Monolithic Refractories. Plibrico Japan Co.,
Tokyo, 1984.
19. Schlegel, E., Sintering of dolomite as a function of the raw material properties. Sprechsaal, 1987, 120, 170–176.
20. Paksocimas, C. A., Varela, J. A., Longo, E. and Whittemore, O. J., The influence of Fe2O3 on stabilization and sintering of MgO stabilized zirconia. In Proceedings of the Fifth International Symposium on the Science and Technology of Sintering. Vancouver, 1991, pp. 23–26.
21. Serry, M. A., Mandour, M. A., Osman, A. M. G. and Girgis, L. G., Low-flux hydration-resistant refractory dolomite grains from Egyptian raw materials. Interceram, 1993, 42, 20–23.
22. Antonov, G. I., Grivakova, Zh. A. and Maslov, A. G., Suitability of Zavadov deposit dolomites for use as raw material. Refract. Ind. Ceram., 1987, 95–100 [translated from Ogneupory].
23. Harabi, A. and Achour, S., A process for sintering of MgO and CaO based ceramics. J. Mater. Sci. Lett., 1999, 18, 955–957.
24. Searle, A. B. and Grimshaw, R. W., The Chemistry and Physics of Clays and other Ceramic Materials. Ernest Benn Limited, London, 1960.
25. Shi. Ying, Y., Messing, G. L. and Bradt, R., Reactive-phase calsintering of calcium-carbonate-derived lime. Commun. Am. Ceram. Soc., 1984, 6, 109–111.
26. Chaudhury, M. N., Kumar, A. and Bhadra, A. K., Microstructure of sintered natural Indian magnesite with titania additions. Ceram. Bull., 1992, 71, 345–348.
27. Marechal, P., Thermal shock resistance of electrofused magnesia grains. Ceram. Bull., 1991, 70, 1780–1782.
28. Green, J., Calcination of precipitated Mg(OH)2 to active MgO in the production of refractory and chemical grade MgO. J. Mater. Sci., 1983, 18, 637–651.
29. Satyoko, Y. and Lee, W. E., Dissolution of dolomite and doloma in silicate slag. Br. Ceram. Trans., 1999, 98, 261–265.
30. White, J., High Temperature Oxides. Part I. Magnesia, Lime and Chrome Refractories, ed. A. M. Alper. Academic Press, New York, 1970.
31. S¸es¸en, K., The Kinetics of Metallurgical Durations. I.T.U. Faculty of Chemical-Metallurgical Ofset Workshop, Istanbul, 1998.
32. Perry, J. H., Chemical Engineering Handbook. McGraw-Hill, New York, 1985.
33. Kappmeyer, K. K., The Importance of Microstructural Considerations in the Performance of Steel Plant Refractories, ed. Fulrath and Pask. Robert Krieger Publishing Company, New York, 1966 [chapter 23]

 FA
FA  EN
EN  AR
AR 